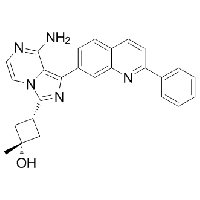
MC81548 OSI-906 (Linsitinib) 867160-71-2 OSI-906 (Linsitinib)
详情
| 英文名称 | 867160-71-2 |
|---|---|
| 别名 | C26H23N5O |
| 分子式 | 421.51 |
| CAS号 | |
| 分子量 | S81548 |
| MDL | OSI-906 (Linsitinib) |
| 名称 | 99% |
| 介绍 | /311328.gif |
文档信息
| 文档 | COA NMR HPLC MSDS Datasheet |
|---|
生物活性
| 描述 | Losmapimod是 IGF-1 和胰岛素受体的双重抑制剂,IC50 分别为35 和 75 nM。 |
|---|---|
| 相关类别 |
信号通路 >> 蛋白酪氨酸激酶 >> IGF-1R 信号通路 >> 蛋白酪氨酸激酶 >> 胰岛素受体 研究领域 >> 癌症 |
| 靶点 |
IC50: 35 nM (IGF-1R), 75 nM (InsR) |
| 体外研究 | Linsitinib抑制IGF-1R自身磷酸化和下游信号蛋白Akt,ERK1 / 2和S6激酶的激活,IC50为0.028至0.13μM。 Linsitinib通过与C-螺旋的相互作用实现靶蛋白的中间构象。 Linsitinib在肝微粒体中显示出有利的代谢稳定性。 Linsitinib在1μM浓度下完全抑制IR和IGF-1R磷酸化。 Linsitinib抑制几种肿瘤细胞系的增殖,包括非小细胞肺癌和结直肠癌(CRC)肿瘤细胞系,EC50为0.021-0.810μM[1]。 |
| 体内研究 | Linsitinib在IGF-1R驱动的异种移植小鼠模型中抑制肿瘤生长,在75mg / kg和60%TGI的剂量下具有100%TGI和55%消退,并且在25mg / kg的剂量下无消退。 Linsitinib给药在狗,大鼠和小鼠中诱导其自身的不同消除半衰期,消除半衰期分别为1.18小时,2.64小时和2.14小时。在雌性Sprague-Dawley大鼠和女性CD-1小鼠中每日一次的不同单剂量的Linsitinib给药显示Vmax与Linsitinib剂量不是剂量成比例的。在给药12天后,Linsitinib以25mg / kg的剂量升高血糖水平。 LIZitinib在IGF-1R驱动的全长人IGF-1R(LISN)异种移植小鼠模型中以75mg / kg的单剂量给药,在4至24小时内用血浆药物实现IGF-1R磷酸化(80%)的最大抑制浓度为26.6-4.77μM[1]。在NCI-H292异种移植物小鼠中以60mg / kg的单剂量施用的Linsitinib在体内治疗后2,4和24小时抑制葡萄糖的摄取。 Linsitinib抑制NCI-H292异种移植小鼠模型中肿瘤的生长[2]。 |
| 激酶实验 | 蛋白激酶测定或者通过基于ELISA的测定方法(IGF-1R,IR,EGFR和KDR)在内部进行,或者通过使用100μM浓度的ATP的放射测定方法进行。内部ELISA测定使用聚(Glu:Tyr)作为与96孔测定板表面结合的底物,并使用与辣根过氧化物酶偶联的抗磷酸酪氨酸抗体检测磷酸化。通过测量405 / 490nm处的吸光度,使用ABTS作为过氧化物酶底物定量结合的抗体。所有测定使用纯化的重组激酶催化结构域人IGF-1R或EGFR的重组酶在昆虫细胞中表达为NH2-末端谷胱甘肽S-转移酶融合蛋白,并在室内纯化。 IC50值由抑制百分比对log10化合物浓度的S形剂量 - 反应曲线确定。除非另有说明,否则使用内部测定进行至少三次一式两份的测量。使用ProfilerProTM激酶选择性测定试剂盒,对一组激酶分析浓度为1μM的Linsitinib。 |
| 细胞实验 | 对于细胞增殖的测定,将细胞接种到含有10%FCS的适当培养基中的96孔板中,并在Linsitinib存在下以各种浓度培养3天。使用CellTiterGlo通过细胞内ATP含量的发光定量来确定细胞生长的抑制。数据表示为最大增殖的一部分,通过将存在不同浓度的Linsitinib时的细胞密度除以仅用载体(DMSO)处理的对照细胞的细胞密度来计算。 |
| 动物实验 | 在指数细胞生长期间从细胞培养瓶中收获细胞,用无菌PBS洗涤两次至合适的浓度,然后皮下植入雌性nu / nu CD-1小鼠的右胁腹。将肿瘤建立至200±50mm 3大小,然后随机分成8只小鼠的治疗组,每组用于功效研究。如所示口服施用Linsitinib或媒介物。所示的%TGI值是整个给药期间的中值%TGI。 505的TGI被认为是重要的。生长延迟计算为TC,T和C是治疗(T)组和对照(C)组中平均肿瘤大小达到初始肿瘤体积的400%的天数。治疗不包括在此计算中。 |
| 参考文献 |
[1]. Mulvihill MJ, et al. Discovery of OSI-906: a selective and orally efficacious dual inhibitor of the IGF-1 receptor and insulin receptor. Future Med Chem. 2009 Sep;1(6):1153-71. [2]. McKinley ET, et al. 18FDG-PET predicts pharmacodynamic response to OSI-906, a dual IGF-1R/IR inhibitor, in preclinical mouse models of lung cancer. Clin Cancer Res. 2011 May 15;17(10):3332-40. [3]. Li W, et al. Effectiveness of inhibitor rapamycin, saracatinib, linsitinib and JNJ-38877605 against human prostate cancer cells. Int J Clin Exp Med. 2015 Apr 15;8(4):6563-7. [4]. Tajima K, et al. Metabolic recovery of lipodystrophy, liver steatosis, and pancreatic β cell proliferation after the withdrawal of OSI-906. Sci Rep. 2017 Jun 23;7(1):4119. [5]. Mayu Kyohara, et al. Serum quantitative proteomic analysis reveals soluble EGFR to be a marker of insulin resistance in male mice and humans. Endocrinology. 2017 Oct 5. |
物理化学性质
| 密度 | 1.4±0.1 g/cm3 |
|---|---|
| 分子式 | C26H23N5O |
| 分子量 | 421.494 |
| 精确质量 | 421.190247 |
| PSA | 89.33000 |
| LogP | 3.23 |
| 折射率 | 1.748 |
英文别名
| 别名 |
cis-3-[8-amino-1-(2-phenyl-quinolin-7-yl)-imidazo[1,5-a]pyrazin-3-yl]-1-methylcyclobutanol OSI-906 (Linsitinib) Kinome_3532 cis-3-(8-amino-1-(2-phenyl-7-quinolinyl)imidazo(1,5-a)pyrazin-3-yl)-1-methylcyclobutanol Cyclobutanol, 3-[8-amino-1-(2-phenyl-7-quinolinyl)imidazo[1,5-a]pyrazin-3-yl]-1-methyl-, cis- Linsitinib cis-3-[8-amino-1-(2-phenylquinolin-7-yl)imidazo[1,5-a]pyrazin-1-yl]-1-methylcyclobutan-1-ol OSI906 cis-3-[8-Amino-1-(2-phenyl-7-quinolinyl)imidazo[1,5-a]pyrazin-3-yl]-1-methylcyclobutanol OSI-906AA OSI-906 |
|---|